XVIII. Čoho je možné sa pri vakcínach proti ochoreniu COVID-19 obávať?
(Čas čítania: 5 minút)
(18.1) Všeobecnou komplikáciou po vakcinácii proti ochoreniu COVID-19 – ktoré vyvoláva vírus SARS-CoV-21 – môže byť vznik ADE (antibody dependent enhancement), teda vznik od protilátok závislého zvýšenia zápalovej odpovede organizmu. Výskyt ADE bol v minulosti potvrdený pri priebehu ochorení, ktoré vyvolávajú vírusy SARS-CoV-1 a MERS-CoV2. Vybrané štúdie na animálnych – teda zvieracích – modeloch zároveň preukázali, že výskyt od protilátok závislého zvýšenia zápalovej odpovede organizmu (ADE) je možné pozorovať aj pri priebehu ochorenia COVID-19. Pritom práve skutočnosť, že samotné ochorenie môže vyvolať výskyt ADE, bola dôvodom, prečo mnohé snahy o vývoj vakcín proti ochoreniam, ktoré spôsobujú vírusy SARS-CoV-1 a MERS-CoV zlyhali – riziko prevyšovalo možné benefity.3, 4 V rámci prevencie proti ochoreniu, ktoré vyvoláva MERS-CoV najmä na Arabskom polostrove a v Afrike sa radšej pristúpilo k celoplošnému očkovaniu tiav, ktoré sú prenášačmi vírusu, než k celoplošnému očkovaniu ľudí.5
(18.2) V niektorých odborných publikáciách sa uvádza, že ADE sa objavuje nezávisle6 od typu vakcíny, a preto by sa úspešná vakcinačná stratégia mala zamerať aj na vyvolanie správnej imunitnej odpovede sprostredkovanej T-lymfocytmi, kedy má imunitná odpoveď voči vírusovému patogénu omnoho promptnejšie a komplexnejšie rozmery s menším rizikom vyvolania ADE. Korelácia medzi rozvojom ADE a konkrétnym typom vakcíny ostáva na úrovni vedeckej pôdy neustále otvorená a bude môcť byť relevantne zodpovedaná až zberom a analýzou ďalších dát.
(18.3) Od protilátok závislé zvýšenie zápalovej odpovede organizmu (ADE) a s ním úzko súvisiaca „cytokínová búrka“ boli pozorované aj pri priebehu ochorenia COVID-19, ak k jeho vyvolaniu došlo reinfekciou novým kmeňom vírusu SARS-CoV-2. Imunitnému systému sa pôvodne vytvorenými protilátkami nepodarilo eliminovať nový kmeň vírusu a zápalová odpoveď organizmu na patogén sa naopak ešte umocnila6A. Ak sa tento fenomén pozoroval pri reinfekcii, nahlas sa zamýšľame, či je pri hľadaní správnej formy prevencie voči vírusu – ktorý údajne podlieha v tak krátkom časovom horizonte mutáciám – správne toto potenciálne riziko vzniku ADE z dlhodobého hľadiska až tak podceňovať. Otvorenou otázkou zostáva, či by nebolo rozumnejšie zamerať sa pri vývoji prevenčných prostriedkov proti ochoreniu COVID-19 na reguláciu T-lymfocytárnej imunitnej dráhy, ktorá má tiež schopnosť dlhodobej pamäte a jej zbraňou v boji proti patogénom nie sú ešte protilátky, teda riziko vzniku ADE odpadá.7
(18.4) Hoci sa podľa informácií uvedených v súhrne charakteristických vlastností vakcíny od Pfizer-BioNTech a Moderna uvádza, že pri testoch na myšiach nebola sledovaná reprodukčná toxicita, štrukturálna podobnosť S proteínu s ľudským syncitínom-1, ktorý je proteínom zodpovedným za vývoj a rast placenty počas tehotenstva, otvára otázku, či sa protilátky tvorené voči S proteínu nebudú tváriť aj ako anti-syncitín-1 protilátky, a teda by mohli spôsobovať problémy u žien počas ich tehotenstva.8
(18.5) Súvis vakcín s následným vývojom autoimunitných ochorení nie je vo vedeckej obci novou témou. Prvýkrát tento stav popísal Dr. Shoenfeld ako ASIA (autoimmune / inflammatory syndrome induced by adjuvants), teda autoimunitný / zápalový syndróm spôsobený adjuvantmi. Okrem adjuvantov vo vakcínach však môže autoimunitné ochorenie spúšťať aj samotný antigén vírusu pri nakazení sa človeka. Jedným z princípov rozvoja autoimunitného ochorenia je princíp tzv. molekulárneho mimikry, kedy sa antigén patogénu, v tomto prípade vírusu SARS-CoV-2, podobá na konkrétny ľudský proteín a pri tvorbe protilátok voči tomuto patogénu sa tvoria protilátky aj voči proteínu bežne vyskytujúcom sa v organizme človeka. Preto pri produkcii vakcín musí byť rozsah molekulárneho mimikry medzi SARS-CoV-2 a ľudskými proteínmi starostlivo analyzovaný.9, 10
(18.6) Európska lieková agentúra a Európska komisia zriadili niekoľko právnych a procedurálnych nástrojov, ktorými je možné urýchliť schvaľovanie tzv. mock-up vakcín, čiže šablónovitých vakcín. V súčasnosti sa to týka najmä vakcín proti pandémii chrípky. Ide o nástroje „autorizácia predaja vakcín pandemickej pripravenosti“ a „núdzová procedúra schvaľovania“ a „procedúra modifikácie vakcíny na sezónnu chrípku“.11 Mock-up vakcína je vakcína, ktorá obsahuje kmeň chrípkového vírusu, ktorý by mohol spôsobiť pandémiu.
(18.7) Mock-up procedúra teda umožňuje vyvinúť vakcínu ešte pred pandémiou. Takéto vakcíny bežne obsahujú kmeň vírusu vtáčej chrípky (napríklad A/H5N1), ktorému bolo vystavených už niekoľko ľudí na svete a ktorý by mohol potenciálne spôsobiť pandémiu. V súčasnosti sú povolené v rámci Európskej únie štyri takéto vakcíny so „základným zložením“, ktoré boli testované na účinnosť. V prípade pandémie môže výrobca po identifikácii vírusového kmeňa spôsobujúceho pandémiu tento kmeň zahrnúť do schválenej „základnej“ mock-up vakcíny a požiadať o schválenie vakcíny ako „konečnej“ pandemickej vakcíny.
(18.8) Vychádza sa z predpokladu, že ak sa nemení chemické, ale len antigénové zloženie, ide o totožnú vakcínu ako je jej predloha a nemôže dôjsť k iným nežiaducim účinkom. Avšak pri vakcínach proti sezónnej chrípke častejší výskyt nežiaducich účinkov z dôvodu reformulácie vakcíny potvrdzuje aj WHO.12 Z tohto dôvodu sa otvára otázka, či aj pri vakcínach proti ochoreniu COVID-19 nemôže kvôli vyskytujúcim sa novým mutáciám vírusu SARS-Cov-2 podobné pozmeňovanie antigénu a podobný princíp schvaľovania, ako je pri vakcínach pre pandémiu chrípky, priniesť rovnaké riziká.
(18.9) Ďalej je potrebné zodpovedne pristupovať k hláseniu a vyhodnocovaniu nežiaducich účinkov vakcín s podmienečným schválením a o týchto vyhodnoteniach informovať pravdivo verejnosť. Podľa Európskej databázy hlásení o podozreniach na nežiaduce účinky liekov boli k 27. 3. 2021 nahlásené do systému EudraVigilance13 podozrenia na nežiaduce účinky podmienečne schválených vakcín proti ochoreniu COVID-19 takto14:
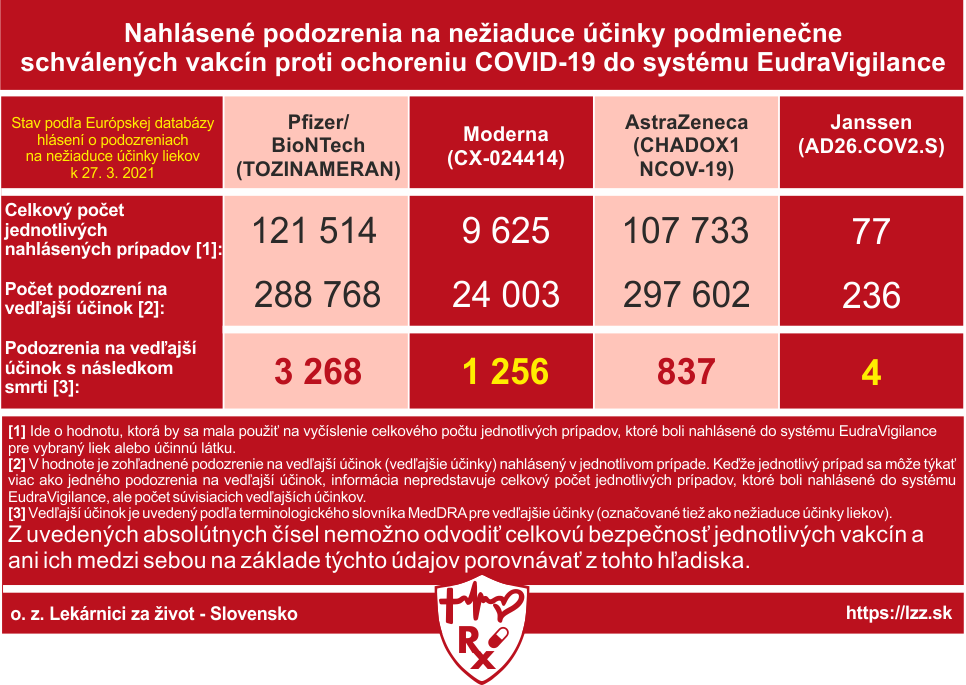 vp.18.1: Nahlásené podozrenia na nežiaduce účinky podmienečne schválených vakcín proti ochoreniu COVID-19 do systému EudraVigilance (k 27. 3. 2021)
vp.18.1: Nahlásené podozrenia na nežiaduce účinky podmienečne schválených vakcín proti ochoreniu COVID-19 do systému EudraVigilance (k 27. 3. 2021)
(18.9.1) Pfizer/BioNTech (TOZINAMERAN):
Celkový počet jednotlivých nahlásených prípadov15: 121 514 z toho 82% z krajín Európskej únie
Počet podozrení na vedľajší účinok16: 288 768
Podozrenia na vedľajší účinok s následkom smrti17: 3 268
(18.9.2) Moderna (CX-024414):
Celkový počet jednotlivých nahlásených prípadov: 9 625 z toho 60,8% z krajín Európskej únie
Počet podozrení na vedľajší účinok: 24 003
Podozrenia na vedľajší účinok s následkom smrti: 1 256
(18.9.3) AstraZeneca (CHADOX1 NCOV-19):
Celkový počet jednotlivých nahlásených prípadov: 107 733 z toho 36,2% z krajín Európskej únie
Počet podozrení na vedľajší účinok: 297 602
Podozrenia na vedľajší účinok s následkom smrti: 837
(18.9.4) Janssen (AD26.COV2.S):
Celkový počet jednotlivých nahlásených prípadov: 77 z toho 1,3% z krajín Európskej únie
Počet podozrení na vedľajší účinok: 236
Podozrenia na vedľajší účinok s následkom smrti: 4
(18.10) Uvedené údaje možno interpretovať tak, že ak sa u pacienta očkovaného konkrétnou vakcínou objaví a nahlási podozrenie na nežiaduci účinok, potom pravdepodobnosť, že pôjde o podozrenie na nežiaduci účinok s následkom smrti je:
(18.10.1) pri vakcíne od Pfizer/BioNTech (TOZINAMERAN): 2,69%
(18.10.2) pri vakcíne od Moderna (CX-024414): 13,05%
(18.10.3) pri vakcíne od AstraZeneca (CHADOX1 NCOV-19): 0,78%
(18.10.4) pri vakcíne od Janssen (AD26.COV2.S): 5,19%

Nie je mi ľahostajné nič z toho, o čom som sa dočítal, a preto sa chcem pridať k verejnej prosbe všetkým slovenským biskupom, aby pred svetom bránili výhradu vo svedomí voči vývoju, dispenzácii, aplikácii a príjmu vakcín vyprodukovaných alebo testovaných na embryonálnych a fetálnych bunkových kultúrach a líniách.

Poznámky a zdroje:





